Калорийность пищи
Содержание:
- Рыба и морепродукты:
- Суточная норма белка
- Марки стали – таблица с маркировкой и расшифровкой
- О чем говорит маркировка сталей
- Что такое пищевая ценность продуктов питания
- Классификация неорганических веществ
- Зелень и овощи
- Генетическая связь между различными классами неорганических соединений
- Структура Периодической системы элементов
- Фрукты, сухофрукты и ягоды
- Химический состав по массе и по объему
- Что такое химические уравнения
- Особенности употребления гречки на диете
- Состав и полезные свойства вареной и сырой свеклы
- Низкоуглеродистые стали
- Общие понятия о марках стали
- Пищевая ценность и калорийность продуктов питания
- Химический состав стали 13Х11Н2В2МФ-Ш (ЭИ961-Ш)
Рыба и морепродукты:
Вобла
Горбуша
Зубатка пестрая
Икра горбуши
Икра красная зернистая
Икра минтая
Икра чёрная зернистая
Кальмар
Камбала
Карась
Карп
Кета
Кижуч
Килька балтийская
Килька каспийская
Краб камчатский (мясо)
Креветка
Лангуст (морской рак)
Лещ
Лосось атлантический (сёмга)
Мидии
Минтай
Мойва
Навага
Нерка красная
Окунь морской
Окунь речной
Осётр
Палтус
Пикша
Путассу
Рак речной
Рыбий жир (из печени трески)
Сазан
Салака
Сельдь жирная
Сельдь нежирная
Скумбрия
Сом
Ставрида
Судак
Треска
Тунец
Угорь
Устрица
Хек
Щука
Готовые блюда из рыбы и морепродуктов:Горбуша натуральная (консервы)
Горбуша отварная
Горбуша соленая
Зубатка жареная
Зубатка отварная
Карп жареный
Кета соленая
Килька горячего копчения
Килька солёная
Килька солёная с луком и маслом
Котлеты из трески
Лещ вяленый
Лещ горячего копчения
Лещ холодного копчения
Навага жареная
Окунь горячего копчения
Окунь жареный
Окунь запеченный
Окунь морской отварной
Печень трески (консервы)
Рак речной вареный
Салака горячего копчения
Сельдь с луком
Скумбрия в масле (консервы)
Скумбрия холодного копчения
Ставрида жареная
Судак отварной
Треска горячего копчения
Треска жареная
Треска запеченная
Треска отварная
Треска тушеная
Тунец в масле (консервы)
Шпроты в масле (консервы)
Щука отварная
Суточная норма белка
Все вы непрерывно нуждаетесь в аминокислотах. Они выполняют свою функцию и распадаются. Часть попадает в кровь и используется вновь, другая часть – утилизируется.
Белки жизненно необходимы. Поэтому каждый взрослый человек должен употреблять минимум 40–50 г белка в сутки.
На самом деле 40–50 г – минимальная норма потребления, которая необходима для вашей жизни.
Ваша потребность зависит от калорийности. Калорийность, в свою очередь, зависит от пола, веса, возраста, физической активности. Рассчитав вашу индивидуальную калорийность и учитывая, что 1 г белка имеет калорийность 4 ккал и рассчитывается ваша норма. Поэтому говорить, что каждому человеку нужно 1, — 1,5 или 2 г белка на 1 кг веса в день — неверно.
Приблизительная норма на день приведена в таблице ниже в граммах.
Для примера были проведены расчёты для мужчины и женщины 30 лет, среднего роста с низкой активностью.
В случае с набором веса взята средняя активность (3 тренировки в неделю).
В зависимости от вашего веса и пола вы можете взять данные из таблицы за основу своего рациона. Повторяюсь, цифра примерная. Подобные расчёты проводятся по определённым формулам, согласно вашему возрасту, росту, весу, активности и ваших целей.
| 50 -55 кг | 55-60 кг | 60-65 кг | 65-70 кг | 75-80 кг | 80-85 кг | |
| Мужчины | ||||||
| Похудение | 145 | 150 | 155 | 160 | 165 | 170 |
| Поддержание веса | 136 | 141 | 145 | 150 | 155 | 160 |
| Набор мышечной массы | 200 | 210 | 220 | 230 | 240 | 250 |
| Женщины | ||||||
| Похудение | 122 | 127 | 132 | 137 | 142 | 147 |
| Поддержание веса | 116 | 120 | 124 | 128 | 132 | 136 |
| Набор мышечной массы | 170 | 177 | 184 | 191 | 198 | 205 |
Здесь имеется в виду не только животный, но и растительный белок. А значит учитывайте не только мясо, яйца, но и хлеб, молочные продукты, крупы, овощи, фрукты и т. д. Поэтому какими бы ни были ваши цели, скорее всего, вам не придётся прилагать огромных усилий для того, чтобы достичь своей нормы.
Когда потребность в белках возрастает
- При увеличении физической нагрузки (тяжёлая работа, тренировки для увеличения мышечной массы и т. д.).
- Во время болезни, и в период выздоровления, а также во время стрессов.
- Во время интенсивного роста и развития.
- При беременности и грудном вскармливании.
- В холодное время года.
Признаки нехватки белка
- Усталость, слабость, утомляемость.
- Снижение объёма мускулатуры.
- Задержка роста у детей.
- Сухая, дряблая кожа.
- Сухие, тусклые, ломкие волосы.
- Снижение сопротивляемости к различным инфекциям.
- Анемия.
- Отёки.
- Нарушение функций систем организма: сердечно-сосудистой, нервной, кровеносной, ЖКТ и т. д.
Причины дефицита
- Нехватка белка в пище.
- Несбалансированность рациона из-за питания только растительной пищей, голодания или вегетарианства. Вы можете есть белковые продукты, но при этом не получать весь комплекс необходимых аминокислот.
- Заболевания ЖКТ.
- Нарушение всасывания.
- Дефицит гормонов.
Избыток белка в организме
Хроническое употребление большого количества белка может вызывать:
- желудочно-кишечные, почечные и сосудистые нарушения;
- снижение естественного иммунитета, что приводит к инфекционным болезням;
- фактор риска возникновения онкологии.
Марки стали – таблица с маркировкой и расшифровкой
Любому специалисту, имеющему дело с металлом, знакомо понятие «марки стали». Расшифровка маркировки стальных сплавов дает возможность получить представление об их химическом составе и физических характеристиках
Разобраться в данной маркировке, несмотря на ее кажущуюся сложность, достаточно просто – важно только знать, по какому принципу она составляется

Редкое производство обходится без стали, поэтому разбираться в его марках крайне важно
Обозначают сплав буквами и цифрами, по которым можно точно определить, какие химические элементы в нем содержатся и в каком количестве. Зная это, а также то, как каждый из таких элементов может влиять на готовый сплав, можно с высокой степенью вероятности определить, какие именно технические характеристики свойственны определенной марке стали.
О чем говорит маркировка сталей
Расшифровать марку стали довольно просто, необходимо только владеть определенными сведениями. Конструкционные стали, обладающие обыкновенным качеством и не содержащие легирующих элементов, маркируют буквосочетанием «Ст». По цифре, идущей после букв в названии марки, можно определить, сколько в таком сплаве углерода (исчисляется в десятых долях процента). За цифрами могут идти буквы «КП»: по ним становится ясно, что данный сплав не до конца прошел процесс раскисления в печи, соответственно, он относится к категории кипящего. Если название марки не содержит таких букв, то сталь соответствует категории спокойной.
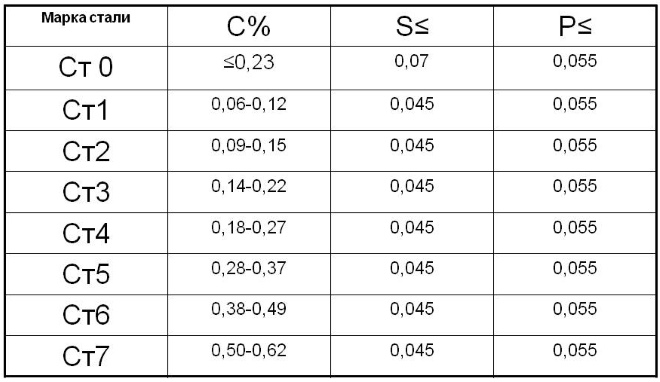
Химический состав углеродистых конструкционных сталей обыкновенного качества
Прежде чем приступить к рассмотрению марок тех сталей, которые включают легирующие добавки, следует разобраться в том, как данные добавки обозначаются. Маркировка легированных сталей может включать такие буквенные обозначения:
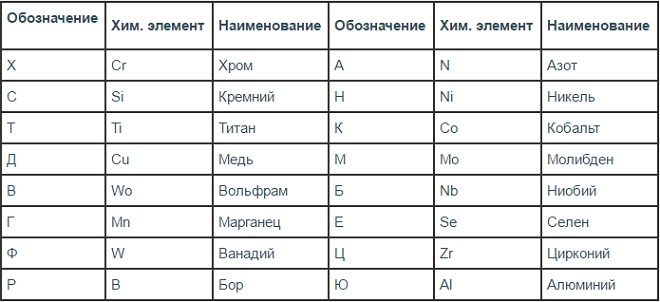
Список используемых легирующих добавок
Что такое пищевая ценность продуктов питания

Это комплексное свойство еды, содержащее определенное количество энергии, которая образовывается при окислении углеводов, жиров и белков. Она необходима для выполнения базовых физиологических и химических функций организма. Любой элемент потребляемой человеком еды, будь она животного или же растительного происхождения, имеет свою калорийность, которая измеряется килокалориями или килоджоулями. Комплекс, который заключается в пищевой ценности продуктов питания, состоит из таких элементов:
- энергетическая ценность;
- биологическая эффективность;
- гликемический индекс;
- физиологическая ценность.
Энергетическая ценность
ЭЦ – количество энергии, высвобождаемой в организме человека при употреблении той или иной пищи. Энергетическая ценность (калорийность) должна примерно совпадать с ее затратами. Изменения в большей или меньшей степени обязательно приведут к неприятным последствиям
Например, регулярное накопление пищевой энергии, превышающее суточные потребности организма – путь к ожирению, поэтому важно рассчитать долю потребляемых жиров, белков и углеводов в зависимости от персональной активности. Это можно сделать онлайн на большинстве сайтов, посвященных диетологии
Биологическая эффективность
Это определение означает показатель качества жировых компонентов в пище, содержание в ней полиненасыщенных кислот, витаминов, прочих необходимых минеральных веществ. В природе этих веществ существует множество, однако для построения организма их необходимо всего 22. Восемь аминокислот являются незаменимыми (не синтезируются самостоятельно):
- метионин;
- лейцин;
- триптофан;
- фенилаланин;
- лизин;
- изолейцин;
- валин;
- треонин.
Гликемический индекс
Помимо калорийности, любой продукт, употребляемый человеком, обладает гликемическим индексом (ГИ). Это условное определение скорости расщепления углеводсодержащей пищи. За норматив принято считать ГИ глюкозы – 100 единиц. Чем быстрее протекает процесс расщепления любого продукта, тем больше его показатель гликемического индекса. Врачи-диетологи пищу подразделяют на группы с высоким (пустые углеводы) и низким (медленные) ГИ.
Физиологическая ценность
Этот элемент пищевой ценности определяется способностью продуктов воздействовать на важные системы организма человека:
- Пектин и клетчатка (балластные вещества) благоприятно влияют на переваривание пищи и проходимость кишечника.
- Алкалоиды кофе и чая возбуждают сердечно-сосудистую и нервную системы.
- Витамины, содержащиеся в продуктах, настраивают иммунитет человеческого организма.
 Калорийность пищевых продуктов.
Калорийность пищевых продуктов.
Смотреть видео
Классификация неорганических веществ
| 1 определение — СЛОЖНЫЕ — состоят из ионов двух или более химических элементов | ПРОСТЫЕ — состоят из атомов одного элемента | ||
| Основания и амфотерные гидроксиды Ме(OH)n |
Кислоты HnК |
Соли MenKm |
Металлы: K, Fe, Ca |
| растворимые в воде (щелочи): NaOH, KOH, Ba(OH)2 |
бескислородные: HCl, HBr, HJ |
средние: K2SO4, NaCl |
Неметаллы: C, S, Si |
| нерастворимые: Cu(OH)2, Fe(OH)3 | кислородсодержащие: HNO3, H2SO4 | Кислые: КHCO3, Ca(H2PO4)2 | Амфотерные: Zn, Al, Cr |
|
Оснóвные: Fe(NO3)OH, Cu2CO3(OH)2 |
Благородные (инертные) газы: Ar, He, Ne | ||
| Двойные: KNaCO3 | |||
| Смешанные: Ca(OCl)Cl | |||
| Комплексные: Na |
Солеобразующие делятся на:
- Оснóвные — образуются при взаимодействии O2 и металлов со степенями окисления +1, +2: K2O, FeO, CuO и др. Оксиды активных металлов при взаимодействии с водой образуют основания. При реакции с кислотами дают соли.
- Кислотные (ангидриды) — образуются при взаимодействии O2с неметаллами: CO2, P2O5 и др, а также металлами со степенью окисления выше, чем +5: Mn2O7, CrO3 и др. При взаимодействии с водой дают кислоты (кроме SiO2). Реагируют с основаниями, образуя соли.
- Амфотерные — образуются при взаимодействии O2 с переходными металлами со степенями окисления: +2: только ZnO, SnO, BeO, PbO; +3: все, кроме La2O3 Al2O3, Fe2O3 и др.; =+4 MoO2, TiO2; +5 V2O5. Взаимодействуют и с кислотами, и с щелочами, дают соли.
- Двойные (солеобразные) — содержат два оксида, где химический элемент проявляет разные степени окисления. При взаимодействии с кислотами двойной оксид показывает и оснóвные, и амфотерные свойства, образуя две различные соли. Например, (Fe2+Fe3+)O4: включает оксиды FeO и Fe2O3. Катионы железа здесь степенях окисления 2+ и 3+: (Fe2+Fe3+2)O4 + 4H2SO4 → FeSO4 + Fe2(SO4)2 + 4H2O.
По агрегатному состоянию оксиды могут быть:
- Твердыми: все оснóвные оксиды, P2O5, Al2O3.
- Жидкими: SO3, Cl2O7 и др.
- Газообразными: CO2, SO2 и др.
В зависимости от растворимости в воде основания подразделяют на:
- Растворимые (щелочи) — образуются щелочными и щелочно-земельными металлами: KOH, RbOH, Ba(OH)2 и др.
- Нерастворимые: Pb(OH)2, Ni(OH)2 и др.
По степени кислотности (число гидроксо-групп) основания могут быть:
- Однокислотными: NaOH, LiOH и др.
- Двухкислотными: Сa(OH)2 и др.
- Трехкислотными: Al(OH)3, Cr(OH)3.
В зависимости от степени диссоциации основания бывают сильные (щелочи, Cа(OH)2 и др.) и слабые (нерастворимые и NH4OH).
Амфотерные гидроксиды: Zn(OH)2, Al(OH)3 имеют свойства и оснований, и кислот.
Кислоты классифицируют по разным признакам:
- Наличие O2 в кислотном остатке: кислородсодержащие (кислородные гидроксиды) — HNO3, H2SO4 и бескислородные — HCl, HBr, HJ.
- Основность (число атомов H, способных замещаться на металл): одноосновные — HNO3, HF; двухосновные: H2CO3, H2S; трехосновные: H3PO4.
- Растворимость в воде: нерастворимые — H2SiO3; растворимые — H2SO4, HNO3.
- Летучесть: нелетучие — H2SO4, H2SiO3 и летучие — HCl, H2S.
MenKm Men++ Km-
KCl =K+ + Cl-;
Al2(SO4)3 = 2Al3++ 3SO42-
Соли бывают следующих видов:
- Средние (нормальные) = катион металла + анион кислотного остатка: Na2CO3, Mg(NO3)2 и т.д.
- Кислые = катион металла + анион кислотного остатка с атомом Н КHCO3, Ca(H2PO4)2 и др.
- Оснóвные (гидроксосоли) = катион металла + гидроксо-группа+анион кислотного остатка: Fe(NO3)OH, Cu2CO3(OH)2 и др.
- Двойные= катионы двух металлов + анион кислотного остатка: CaMg(CO3)2, KAl(SO4)2 и др.
- Смешанные= катион металла + два разных кислотных остатка: Ca(OCl)Cl, CuBrCl и др.
- Комплексные= комплексный катион или анион — атом металла + несколько лиганд: Na2ZnCl4 и др.
Зелень и овощи
Внимание! Чтобы увидеть всю таблицу, выберите «Показать 50 записей» или воспользуйтесь кнопками «Предыдущая» и «Следующая» для просмотра таблицы по частям
| Продукт | Калорийность | Белки | Жиры | Углеводы |
| Баклажаны | 24 | 0,6 | 0,1 | 5,5 |
| Брюква | 37 | 1,2 | 0,1 | 8,1 |
| Горошек зеленый | 72 | 5,0 | 0,2 | 13,3 |
| Кабачки | 27 | 0,6 | 0,3 | 5,7 |
| Капуста белокочанная | 28 | 1,8 | 5,4 | |
| Капуста краснокочанная | 31 | 1,8 | 6,1 | |
| Капуста цветная | 29 | 2,5 | 4,9 | |
| Картофель | 83 | 2 | 0,1 | 19,7 |
| Лук зеленый (перо) | 22 | 1,3 | 4,3 | |
| Лук порей | 40 | 3 | 7,3 | |
| Лук репчатый | 43 | 1,7 | 9,5 | |
| Морковь красная | 33 | 1,3 | 0,1 | 7 |
| Огурцы грунтовые | 15 | 0,8 | 3 | |
| Огурцы парниковые | 10 | 0,7 | 1,8 | |
| Перец зеленый сладкий | 23 | 1,3 | 4,7 | |
| Перец красный сладкий | 27 | 1,3 | 5,7 | |
| Петрушка (зелень) | 45 | 3,7 | 8,1 | |
| Петрушка (корень) | 47 | 1,5 | 11 | |
| Ревень (черешковый) | 16 | 0,7 | 2,9 | |
| Редис | 20 | 1,2 | 4,1 | |
| Редька | 34 | 1,9 | 7 | |
| Репа | 28 | 1,5 | 5,9 | |
| Салат | 14 | 1,5 | 2,2 | |
| Свекла | 48 | 1,7 | 10,8 | |
| Томаты (грунтовые) | 19 | 0,6 | 4,2 | |
| Томаты (парниковые) | 14 | 0,6 | 2,9 | |
| Зелёная фасоль | 32 | 4 | 4,3 | |
| Хрен | 71 | 2,5 | 16,3 | |
| Черемша | 34 | 2,4 | 6,5 | |
| Чеснок | 106 | 6,5 | 21,2 | |
| Шпинат | 21 | 2,9 | 2,3 | |
| Щавель | 28 | 1,5 | 5,3 |
Генетическая связь между различными классами неорганических соединений
Между классами неорганических веществ существует генетическая связь: из веществ одного класса можно получить вещества другого. Это отражено в генетических рядах превращений, которые могут идти двумя путями:
- Начиная с металла (если он образует растворимое основание — щелочь). Например, из простого вещества получают оксид, затем щелочь, потом соль и снова металл: Na → Na2O → NaOH → Na2SO4 → Na — полный генетический ряд натрия. Для металлов, которые образуют нерастворимые основания, после получения оксида сначала получают соль, затем основание: Zn → ZnO → ZnSO4→Zn(OH)2↓ — неполный генетический ряд цинка. Чтобы ряд считался полным, нужно добавить превращение Zn(OH)2 → Zn.
- Начиная с неметалла, например, из простого вещества поэтапно получают кислотные оксиды, кислоту, потом соль и снова неметалл. S → SO2→ SO3→ H2SO4 → Na2SO4 → S — полный генетический ряд серы.
Главные признаки генетических рядов:
- Все вещества одного ряда должны быть образованы одним химическим элементом.
- Вещества, участвующие в реакциях одного генетического ряда, должны принадлежать к разным классам химических соединений.
В цепочках превращений бывают задействованы и органические соединения, поэтому генетические связи очень многообразны.
Структура Периодической системы элементов
Периодическая таблица химических элементов
На настоящий момент Периодическая таблица Менделеева содержит 118 химических элементов. Каждый из них занимает своё место в зависимости от атомного числа. Оно показывает, сколько протонов содержит ядро атома элемента и сколько электронов в атоме находятся вокруг него. Атом каждого последующего элемента содержит на один протон больше, чем предыдущий.
Периоды — это строки таблицы. На данный момент их семь. У всех элементов одного периода одинаковое количество заполненных электронами энергетических уровней.
Группы — это столбцы. В группы в Периодической таблице объединяются элементы с одинаковым числом электронов на внешнем энергетическом уровне их атомов. В кратком варианте таблицы, используемой в школьных учебниках, элементы разделены на восемь групп. Каждая из них делится на главную (A) и побочную (B) подгруппы, которые объединяют элементы со сходными химическими свойствами.
.jpg)
Каждый элемент обозначается одной или двумя латинскими буквами. Порядковый номер элемента (число протонов в его ядре) обычно пишется в левом верхнем углу. Также в ячейке элемента указана его относительная атомная масса (сумма масс протонов и нейтронов). Это усреднённая величина, для расчёта которой используются атомные массы всех изотопов элемента с учётом их содержания в природе. Поэтому обычно она является дробным числом.
Чтобы узнать количество нейтронов в ядре элемента, необходимо вычесть его порядковый номер из относительной атомной массы (массового числа).
Фрукты, сухофрукты и ягоды
Внимание! Чтобы увидеть всю таблицу, выберите «Показать 100 записей» или воспользуйтесь кнопками «Предыдущая» и «Следующая» для просмотра таблицы по частям
| Продукт | Калорийность | Белки | Жиры | Углеводы |
| Абрикосы | 46 | 0,9 | 10,5 | |
| Авокадо | 223 | 1,9 | 23,5 | 6,7 |
| Айва | 38 | 0,6 | 8,9 | |
| Алыча | 34 | 0,2 | 7,4 | |
| Ананас | 48 | 0,4 | 11,8 | |
| Апельсин | 38 | 0,9 | 8,4 | |
| Арбуз | 38 | 1 | 8 | |
| Бананы | 91 | 1,5 | 22,4 | |
| Брусника | 40 | 0,7 | 8,6 | |
| Виноград | 69 | 0,4 | 17,5 | |
| Вишня | 49 | 0,8 | 11,3 | |
| Вишня (сушёная) | 292 | 1,5 | 73 | |
| Голубика | 37 | 1 | 7,7 | |
| Гранат | 52 | 0,9 | 11,8 | |
| Грейпфрут | 35 | 0,9 | 7,3 | |
| Груша | 42 | 0,4 | 10,7 | |
| Груша (сушёная) | 246 | 2,3 | 62,1 | |
| Ежевика | 33 | 2 | 5,3 | |
| Земляника | 41 | 1,8 | 8,1 | |
| Изюм с косточкой (сушёный) | 276 | 1,8 | 70,9 | |
| Изюм кишмиш (сушёный) | 279 | 2,3 | 71,2 | |
| Инжир | 56 | 0,7 | 13,9 | |
| Калина | 32 | 0,5 | 4,6 | |
| Киви | 61 | 1 | 11 | |
| Кизил | 45 | 1 | 9,7 | |
| Клюква | 28 | 0,5 | 4,8 | |
| Крыжовник | 44 | 0,7 | 9,9 | |
| Курага | 272 | 5,2 | 65,9 | |
| Лимон | 31 | 0,9 | 3,6 | |
| Мандарин | 38 | 0,8 | 8,6 | |
| Малина | 41 | 0,8 | 9 | |
| Морошка | 31 | 0,8 | 6,8 | |
| Облепиха | 30 | 0,9 | 5,5 | |
| Персики | 44 | 0,9 | 10,4 | |
| Персики (сушёные) | 275 | 3,0 | 68,5 | |
| Рябина садовая | 58 | 1,4 | 12,5 | |
| Рябина черноплодная | 54 | 1,5 | 12 | |
| Слива садовая | 43 | 0,8 | 9,9 | |
| Слива сушёная (чернослив) | 264 | 2,3 | 65,6 | |
| Смородина белая | 39 | 0,3 | 8,7 | |
| Смородина красная | 38 | 0,6 | 8 | |
| Смородина черная | 40 | 1,0 | 8,0 | |
| Урюк | 278 | 5 | 67,5 | |
| Финики | 281 | 2,5 | 72,1 | |
| Хурма | 62 | 0,5 | 15,9 | |
| Черешня | 52 | 1,1 | 12,3 | |
| Черника | 40 | 1,1 | 8,6 | |
| Шиповник свежий | 101 | 1,6 | 24 | |
| Шиповник (сушеный) | 253 | 4,0 | 60 | |
| Шелковица | 53 | 0,7 | 12,7 | |
| Яблоки | 46 | 0,4 | 11,3 | |
| Яблоки (сушёные) | 273 | 3,2 | 68 |
Химический состав по массе и по объему
Состав химических соединений, а также состав смесей различных веществ и растворов выражают в массовых долях (массовых %), а состав смесей жидкостей и газов, кроме того, в объемных долях (объемных %).
Состав сложного вещества, выраженный через массовые доли химических элементов, называется составом вещества по массе.
Например, состав Н2О по массе:
То есть, можно сказать, что химический состав воды (по массе): 11,11% водорода и 88,89% кислорода.
Массовая доля компонента в механической смеси (W) – это число, показывающую, какую часть смеси составляет масса компонента от общей массы смеси, принятой за единицу или 100%.
W1 = m1/m(cм.), m(см.) = m1 + m2+ …. mn,
Где m1 – масса 1-го (произвольного)компонента, n – число компонентов смеси, m1 … mn – массы компонентов, образующих смесь, m(cм.) – масса смеси.
Например, массовая доля основного компонента:
W(осн. комп) = m(осн. комп)/m(см.)
Массовая доля примеси:
W(прим.) = m(прим)/m(см.)
Сумма массовых долей всех компонентов, образующих смесь равна 1 или 100%.
Объемная доля газа (или жидкости) в смеси газов (или жидкостей) – это число, показывающее, какую часть по объему составляет объем данного газа (или жидкости) от общего объема смеси, принятого за 1 или за 100%.
Состав смеси газов или жидкостей, выраженный в объемных долях, называется составом смеси по объему.
Например, состав смеси сухого воздуха:
- По объему: Wоб(N2) = 78,1%, Wоб(O2) = 20,9%
- По массе: W(N2) = 75,5%, W(O2) = 23,1%
Этот пример наглядно демонстрирует, что во избежание путаницы, корректно будет всегда указывать, по массе или по объему указано содержание компонента смеси, ведь эти цифры всегда отличаются: по массе в воздушной смеси кислорода получается 23,1 %, а по объему – всего 20,9%.
Растворы можно рассматривать как смеси из растворенного вещества и растворителя. Поэтому их химический состав, как и состав любой смеси, можно выражать в массовых долях компонентов:
W(раств. в-ва) = m(раств. в-ва)/m(р-ра),
где
m(р-ра) = m(раств. в-ва) + m(растворителя)
или
m(р-ра) = p(р-ра)·V(р-ра)
Состав раствора, выраженный через массовую долю растворенного вещества (в %), называется процентной концентрацией этого раствора.
Состав растворов жидкостей в жидкостях (например, спирта в воде, ацетона в воде) удобнее выражать в объемных долях:
Wоб%(раств. ж) = V(раств.ж)· V(р-ра)·100%;
где
V(р-ра) = m(р-ра)/p(р-ра)
или приближенно
V(р-ра) ≈ V(H2O) + V(раств. ж)
Например, содержание спирта в винно-водочных изделиях указывают не в массовых, а в объемных долях (%) и называют эту цифру крепостью напитка.
Состав растворов твердых веществ в жидкостях или газов в жидкостях в объемных долях не выражают.
Что такое химические уравнения
Когда химические вещества вступают во взаимодействие, химические связи между их атомами разрушаются и образуются новые, уже в других сочетаниях. В результате одни вещества превращаются в другие.
Рассмотрим реакцию горения метана, происходящую в конфорке газовой плиты:
.jpg)
Молекула метана (CH₄) и две молекулы кислорода (2O₂) вступают в реакцию, образуя молекулу углекислого газа (CO₂) и две молекулы воды (2H₂O). Связи между атомами углерода (С) и водорода (H) в метане, а также между атомами кислорода (O) разрываются, и образуются новые связи между атомами углерода и кислорода в молекуле углекислого газа (CO₂) и между атомами водорода и кислорода в молекуле воды (H₂O).
Картинка даёт наглядное представление о том, что произошло в ходе реакции. Но зарисовывать сложные химические процессы такими схемами неудобно. Вместо этого учёные используют уравнения химических реакций.
Химическое уравнение — это условная запись химической реакции с помощью формул и символов.
Их записывают в виде схемы, в которой отражён процесс превращения. В левой части располагаются формулы реагентов — веществ, вступающих в реакцию. Завершается уравнение продуктами реакции — веществом или веществами, которые получились в результате.
Новые вещества образуются потому, что изменяются связи между атомами, но сами атомы не возникают из ниоткуда и не исчезают в никуда. На рисунке видно, что атом углерода из состава метана перешёл в состав углекислого газа, атом водорода — в состав воды, а атомы кислорода распределились между молекулами углекислого газа и воды. Число атомов не изменилось.
Согласно закону сохранения массы, общая масса реагентов всегда равна общей массе продуктов реакции. Именно поэтому запись химической реакции называют уравнением.
<<Форма демодоступа>>
Особенности употребления гречки на диете
Гречневая каша — один из самых распространенных продуктов, который используют при диетическом питании. Благодаря высокому содержанию пищевых волокон, аминокислот, антиоксидантов и углеводов гречка способствует похудению.
Можно ли похудеть на гречке
Гречневая диета при правильном подходе способствует потере лишнего веса, а также благоприятно влияет на организм в целом.
Особенности гречневой диеты:
- углеводы расщепляются медленно, а на их переваривание организм тратит много энергии;
- высокая калорийность дает ощущение сытости и исключает истощение;
- гречка очищает стенки желудка, налаживает пищеварение и рассасывает висцеральный жир;
- ускоряет метаболизм, благодаря чему человек теряет лишний вес:
- выводит лишнюю воду и токсины.
Существуют разнообразные диеты на основе гречки:
- по срокам: 3-дневная, недельная, 2-недельная;
- по продуктам: куриная, овощная, молочная, яблочная;
- на воде и гречке (применяют в качестве разгрузочного дня);
- лечебная;
- строгая;
- облегченная.
Чаще всего гречку используют во время монодиеты, но иногда желающие похудеть добавляют в рацион овощи и кисломолочные продукты. Благодаря такому способу удается скинуть до 10 кг за 2 недели при условии выполнения физических нагрузок и сохранения водного баланса.
Рекомендации при соблюдении диеты:
- пить воду — примерно 30-40 мл на 1 кг веса;
- не есть за 5 часов до сна;
- гречку лучше запаривать — так она сохраняет больше питательных веществ;
- при сильном чувстве голода выпивать 1 ст. кефира или есть яблоко;
- вместо кофеина, который задерживает воду в организме, пить травяные чаи.
Примерный вариант гречневой монодиеты:
- утром выпить 1 ст. воды;
- спустя полчаса съесть порцию каши, запаренной кипятком;
- на обед — запаренную гречку с зелеными овощами;
- на ужин — порцию гречневой каши;
- в перерывах пить воду.
Максимальный срок диеты на гречке — 2 недели. Оптимальный вариант — 5-7 дней один раз в 6 месяцев. При этом занимайтесь легкими видами спорта, высыпайтесь и пейте больше воды.
Противопоказания гречневой диеты
Несмотря на полезные свойства продукта, при неправильном соблюдении диеты могут возникнуть проблемы со здоровьем.
Такой вариант похудения имеет свои минусы:
- понижение давления;
- головная боль;
- быстрая утомляемость;
- перепады настроения.
С осторожностью соблюдать диету необходимо людям, у которых:
- болезни желудочно-кишечного тракта;
- сахарный диабет;
- онкология;
- проблемы с обменом веществ;
- болезни сердца;
- индивидуальная непереносимость;
- заболевания почек.
Что будет, если есть только гречку каждый день
По словам врачей и диетологов, ежедневное употребление гречки не нанесет вреда, если употреблять ее с молочными продуктами, овощами, фруктами. За счет высокой калорийности организм будет обеспечен достаточным количеством энергии, а чувство голода будет возникать реже.
Такой рацион обеспечит организм всеми необходимыми минералами, аминокислотами, антиоксидантами. Чтобы поддерживать здоровье, рекомендуется чередовать гречку с другими кашами и крупами.
Состав и полезные свойства вареной и сырой свеклы
Овощ имеет большое количество полезных свойств, которые применяются уже довольно длительное время, к таковым необходимо отнести:
- Насыщение организма полезными минералами, витаминами
- В продукте сдержится полезный элемент — кварц, который необходим для поддержания нормального состояния костей и сосудов
- Применяется для вывода токсинов, шлаков
- Способствует усилению мозговой деятельности
- При выявлении недостаточного уровня гемоглобина рекомендовано употреблять овощ
- Свёкла в сыром виде является эффективным средством для профилактики заболеваний сердца и сосудов.
- Выводит естественным путем вредный холестерин и снимет возможность возникновения тромбов в кровеносных сосудах
- При частых запорах применяется в качестве слабительного средства
- Улучшает обмен веществ в организме, рекомендуется при различных заболеваниях желудка.
Состав вареной и сырой свёклы практически ни чем не отличаются друг от друга, единственные отличия — это тот факт, что при обработке овощ теряет некоторые виды витаминов, а именно: С, В5, фолиевую кислоту. Остальные составляющие продукта хорошо сохраняются как в сыром, так и в вареном виде.
Овощ содержит следующие полезные элементы:
- Витамины группы А, В, С
- Витамины Е, РР
- Железо
- Калий
- Кальций
- Фосфор
- Цинк
- Органические кислоты
Полезно знать! Если рассматривать пользу вареной свёклы и сырой, то все мнения могут быть разнообразны. Обработанный продукт освобождается от возможного наличия различных видов нитратов, а также вредных веществ.
В то время как сырой вид продукта содержит вдвое больше витаминов, что важно клетчаткой, которая в сыром овоще имеет большую силу влияния на организм человека
Низкоуглеродистые стали
50 ХГА (аналог 5160) – марка, пользующаяся большим спросом в кузнечном деле, в частности при изготовлении крупных клинков, с повышенными требованиями к прочности. Для облегчения закаливаемости в этот сплав добавлен хром, количество которого, однако не настолько высокое, чтобы придавать антикоррозионные свойства. Углерода в этой марке содержится примерно 0,6%.
Российская сталь ШХ15 (52100 по американским стандартам) относится к маркам, которые больше подходят для производства охотничьих ножей. Уступает в прочности предыдущей марке, но при этом превосходит ее в способности держать заточку.
В кустарном производстве применяют, как правило, более «трудоемкие» марки. Это могут быть рессорно-пружинные конструкционные стали типа 65Г (аналог – американская сталь 770). Литера «Г» подразумевает наличие марганца в сплаве. Температура ковки от 760 °С до 1250 °С. При содержании марганца свыше 1% данная марка склонна к отпускной хрупкости. Охлаждение производится на воздухе. Популярна в силу своей дешевизны.
Общие понятия о марках стали
На территории СНГ применяемые стандарты обозначений характеризуются тем, что могут использоваться для указания основных элементов. При рассмотрении вопроса расшифровки марки отметим следующие моменты:
- Часто проставляется сокращение «Ст». В других случаях и вовсе не ставится никаких сокращений, только цифры.
- В большинстве случаев первая цифра указывает на концентрацию углерода. Последующие могут применяться для указания количества легирующих компонентов.
- В состав могут включаться легирующие компоненты, которые существенно изменяют свойства материала. Примером можно назвать включение хрома, за счет чего повышается устойчивость к воздействию повышенной влажности.
Классификация сталей по назначению
Расшифровка маркировки проводится при использовании таблиц, в которых указывается обозначение химического элемента.
Пищевая ценность и калорийность продуктов питания
Молочка
| Продукт | Калорийность, ккал/100 г | Б | Ж | У |
| Молоко 3,2% | 57 | 2,8 | 3,2 | 4,8 |
| Творог 9% | 150 | 16,7 | 9,1 | 2,0 |
| Сыр 45% в сухом веществе | 365 | 26,3 | 26,6 | |
| Сметана 15% | 150 | 2,6 | 15 | 28 |
Мясо и яйца
| Продукт | Калорийность, ккал/100 г | Б | Ж | У |
| Свинина | 260 | 18,3 | 21,6 | |
| Говядина | 158 | 22,17 | 7,07 | |
| Курица (бедро) | 160 | 16,8 | 10,2 | |
| Курица (грудка) | 110 | 23,1 | 1,2 | |
| Баранина | 209 | 15,6 | 16,3 | |
| Индейка (бедро) | 243 | 14,72 | 6,4 | |
| Яйца | 158 | 12,7 | 10,9 |
Рыба и морепродукты
Морепродукты содержат большое количество белка.
| Продукт | Калорийность, ккал/100 г | Б | Ж | У |
| Горбуша | 149 | 20,5 | 6,5 | |
| Минтай | 72 | 15,9 | 0,9 | |
| Хек | 86 | 16,6 | 2,2 | |
| Сельдь | 159 | 16,3 | 10,7 | |
| Кальмары | 73 | 18,0 | 0,3 |
Крупы
| Крупа | Калорийность, ккал/100 г | Б | Ж | У |
| Рисовая | 330 | 7,0 | 1,0 | 71,4 |
| Гречневая | 334 | 12,6 | 3,3 | 62,1 |
| Манная | 328 | 10,3 | 1,0 | 67,7 |
| Овсяная | 365 | 11,9 | 7,2 | 69,3 |
| Перловая | 349 | 9,3 | 1,1 | 66,5 |
Хлебобулочные изделия
| Продукт | Калорийность, ккал/100 г | Б | Ж | У |
| Хлеб ржаной | 215 | 5,9 | 1,0 | 44,2 |
| Хлеб пшеничный | 253 | 7,9 | 1,0 | 53,0 |
| Батон | 368 | 7,5 | 1,5 | 70,0 |
| Макароны | 335 | 10,7 | 1,3 | 68,5 |
Овощи
| Виды овощей | Калорийность, ккал/100 г | Б | Ж | У |
| Морковь | 32 | 1,3 | 0,1 | 6,9 |
| Картофель | 80 | 2,0 | 0,4 | 16,3 |
| Огурец | 15 | 0,8 | 0,1 | 3,7 |
| Помидор | 24 | 1,1 | 0,2 | 5,0 |
Фрукты
| Фрукт | Калорийность, ккал/100 г | Б | Ж | У |
| Яблоко | 37 | 0,2 | 0,3 | 8,0 |
| Груша | 43 | 0,4 | 0,3 | 9,5 |
| Банан | 96 | 1,5 | 0,5 | 21,0 |
| Апельсин | 38 | 0,9 | 0,2 | 8,1 |
Химический состав стали 13Х11Н2В2МФ-Ш (ЭИ961-Ш)
| НТД | C | S | P | Mn | Cr | W | V | Ti | Si | Ni | N | Mo | Cu | Al |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ОСТ 1 90090-79 | 0,12-0,16 | ≤0,025 | ≤0,025 | 0,30-0,80 | 10,50-12,00 | 1,50-2,00 | 0,18-0,30 | ≤0,050 | 0,20-0,65 | 1,40-1,80 | ≤0,050 | 0,35-0,50 | ≤0,30 | ≤0,10 |
| ГОСТ 5632-2014 | ≤0,10-0,16 | ≤0,025 | ≤0,030 | ≤0,60 | 10,50-12,00 | 1,60-2,00 | 0,18-0,30 | ≤0,20 | ≤0,60 | 1,50-1,80 | — | 0,35-0,50 | ≤0,30 | — |
| ТУ 14-1-2902-80, ТУ 14-1-2918-80 | ≤0,10-0,16 | ≤0,015 | ≤0,030 | ≤0,60 | 10,50-12,00 | 1,60-2,00 | 0,18-0,30 | ≤0,20 | ≤0,60 | 1,50-1,80 | — | 0,35-0,50 | ≤0,30 | — |
| ТУ 14-1-3297-82 | ≤0,10-0,16 | ≤0,025 | ≤0,030 | ≤0,60 | 10,50-12,00 | 1,60-2,00 | 0,18-0,30 | ≤0,20 | ≤0,60 | 1,50-1,80 | — | 0,35-0,50 | ≤0,25 | — |
По ТУ 14-1-2902-80 химический состав приведен для стали марки 13Х11Н2В2МФ-Ш (ЭИ961-Ш).
По ТУ 14-1-3297-82 химический состав приведен для стали марки 13Х11Н2В2МФ-Ш (ЭИ961-Ш). По требованию потребителя может быть изготовлена сталь марки 13Х11Н2В2МФ-Ш «селект» с содержание элементов С=0,12-0,15%, Ni=1,70-2,00%, V=0,16-0,26%.
По ОСТ 1 90090-79 химический состав приведен для стали марки 13Х11Н2В2МФЛ (ЭИ961Л).
По ТУ 14-1-2918-80 химический состав приведен для стали марки 13Х11Н2В2МФ-Ш (ЭИ961-Ш).








